世界卫生组织4月13日公布的数据显示,全球新冠肺炎累计确诊病例达到1773084例。面对新冠病毒这个全人类的敌人,疫苗才是致胜的终极手段。全球科学家都在争分夺秒研发疫苗,疫苗研发的进度万众瞩目。
新冠疫情发生后,中国立即启动疫苗研发计划,沿着五条疫苗技术路线全力推进。
昨天,一个重大利好消息发布:4月12日,由国药集团中国生物武汉生物制品研究所(以下简称武汉生物制品研究所)申报的一类新药——新型冠状病毒灭活疫苗,获得国家药品监督管理局临床试验许可,这是全球首个获得临床试验批件的新冠病毒灭活疫苗。
临床试验,这是一个来之不易的阶段性成果。目前该疫苗相关临床试验已经启动,并根据国家相关法律法规规定,为应急使用做好充分准备。中国生物相关负责人表示,下一步,将加速科研攻关,力争早日完成临床试验研究,尽快制备安全有效的新冠疫苗,为战胜新冠疫情,保障人类公共卫生安全作出新的贡献。
在全球疫苗研发的过程中,国药集团中国生物能在全球各路军团“并跑”竞赛中,在灭活疫苗技术路线上实现了“领跑”,首家获得临床试验批件,其背后的秘密是什么?经历了什么样的困难和挑战?记者第一时间就此作了深入的采访。
战时速度:集中力量办大事基础上的重大突破
新冠肺炎疫情发生以来,党中央、国务院对疫苗研发攻关高度重视,习近平总书记、李克强总理等党和国家领导人亲自部署科研工作,多次考察了解研发进展情况,要求发挥举国体制优势,加快推进已有的多种技术路线疫苗研发,力争早日推动疫苗的临床试验和上市使用。
据了解,我国新冠病毒疫苗应急攻关按照灭活疫苗、重组蛋白疫苗、腺病毒载体疫苗、减毒流感病毒载体活疫苗、核酸疫苗5条技术路线推进。3月16日,军事科学院军事医学研究院的腺病毒载体疫苗已获批开展一期临床试验。
国药集团作为以医药健康产业为主业的中央企业,在新冠疫苗研发过程中,承担了重要的使命。1月19日,中国生物成立了由科技部“863”计划疫苗项目首席科学家杨晓明挂帅的科研攻关领导小组,以战时节奏,迅速安排了10亿元研发资金,布局三个研究所,集中力量,在两条技术路线上开发新冠病毒疫苗。
其中,一条技术路线是灭活疫苗,由武汉生物制品研究所与中国科学院武汉病毒研究所在武汉协同攻关、密切合作开展研发,国药集团中国生物北京生物制品研究所与中国疾病预防控制中心病毒病预防控制所以及中国食品药品检定研究院共同奋战、高效协作,在北京研发;一条技术路线是基因工程疫苗,由中国生物技术研究院牵头推进。
4月12日,武汉生物制品研究所申报的一类新药——新型冠状病毒灭活疫苗,获得国家药品监督管理局临床试验许可,这是全球首个获得临床试验批件的新冠病毒灭活疫苗。
这样的成绩来之不易!它的背后,是武汉生物制品研究所科研攻关团队3个月的持续奋战和努力。
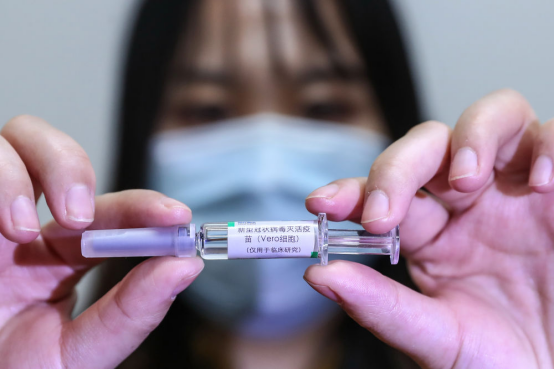
4月10日,工作人员在国药集团中国生物新冠疫苗生产基地展示新型冠状病毒灭活疫苗样品。
争分夺秒:三个月夜以继日加班加点的科研攻关
1月5日,武汉生物制品研究所的合作方——中科院武汉病毒所成功分离新冠病毒毒株,新冠病毒灭活疫苗的研发工作也由此开始。
武汉生物制品研究所有限责任公司病毒性疫苗研究一室主任王泽鋆告诉《国资报告》记者,1月主要开展了两方面的工作,一方面,是病毒在细胞上的适应传代工作的研究,另一方面,由于要研发的是灭活疫苗,因此,需要确定病毒的灭活工艺和灭活条件,以确保疫苗可以灭活成功。
2月1日,国药集团中国生物作为牵头单位,获得了科技部国家重点研发计划“公共安全风险防控与应急技术装备”重点专项“2019-nCoV灭活疫苗”项目的紧急立项,科研攻关团队继续加班加点,将工作向前推进。
2月14日,科研攻关团队获得了纯化抗原,2月16起,开始在大鼠、小鼠、豚鼠,及恒河猴、食蟹猴等多种试验动物身上开展疫苗的免疫原性研究,以验证疫苗的有效性。
2月25日,科研攻关团队开始进行保护性研究,即先给动物注射疫苗,再用病毒让动物感染,看疫苗能否产生免疫力,保护动物不受感染。“保护性研究一直进行到4月7号,在恒河猴等动物身上的试验证明,疫苗有很好的保护效果。”王泽鋆说。
从3月8日开始,科研攻关团队开展了安全性评价工作。“在疫苗研发过程中,有一个重要的环节,就是临床前的安全性评价,即首先要证明疫苗在动物身上是安全的。”王泽鋆说,“这项工作一直持续到4月7号,结果非常理想,没有出现任何异常反应和不良反应。”
毒种是研发和制备疫苗的基础。科研攻关团队同步开展了毒种库的建设工作,按照相关规定,2月28日建立了三级毒种库,开始临床注册批生产疫苗,并在3月18日完成了三批疫苗的生产。“三批疫苗的生产很重要,因为我国要求在申请临床试验之前,必须连续生产三批合格的样品。”王泽鋆说说。4月4日,武汉生物制品研究所生产的灭活疫苗自检合格,4月9日,获得了中国食品药品检定研究院的检定合格报告。
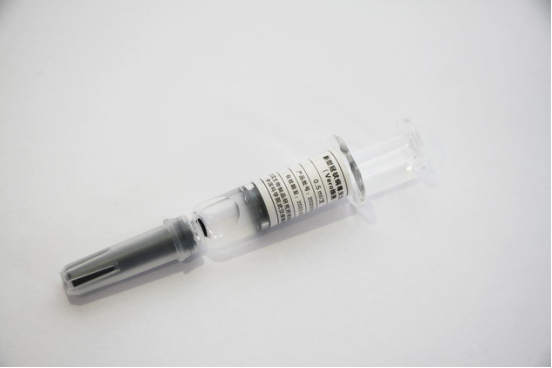
由武汉生物制品研究所与中国科学院武汉病毒研究所协同研发的新冠病毒灭活疫苗。
攻坚克难:从“串联”到“并联”特事特办的工作效率
值得注意的是,由于新冠病毒灭活疫苗的研发攻关时间紧,任务重,科研攻关团队在局部研发环节,由以往的“串联式”变为“并联式”,在尊重研发规律的同时,提升了研发的效率——这意味着更高的工作强度和更集中的投入。
比如在疫苗的有效性评价环节,以往的方式,是对不同种类的动物逐一进行有效性试验,采用并联的方式后,则是同时对不同种类的动物开展有效性试验。
再如,疫苗制备完成后,以往是研发机构要先自己检定合格,再送到中国食品药品检定研究院进行检定,现在则是在研发机构自己检定的同时,送到中检院进行检定,以缩短检验周期。
局部并联的研发方式,提高了研发效率,也让科研团队付出了更多的辛劳。
“不同种类的动物,需要在不同的时间点进行有效性评价,工作的强度可想而知。”王泽鋆说,“我们每天工作都在16个小时以上,相当于把一天当成2天、3天来用。”
在开展灭活疫苗科研攻关的同时,应急审批的工作也在同步进行之中。为使疫苗早日研发成功,国家药监局为疫苗研发机构开通了绿色通道,以往需要将申报材料备齐,一次性提交,现在研发机构可以备好一部分,就提交一部分,以滚动的方式进行提交,国家药监局则同步进行审核,以提高审批速度。
4月10日,武汉生物制品研究所将最终版的申报材料按要求进行了提交,4月12日,获得了国家药监局的临床试验许可。
直面挑战:非常时期克服重重阻力的非常之举
武汉生物制品研究所开展新冠病毒灭活疫苗研发,正值疫情防控阻击战的关键时期,科研攻关团队的所在地,又是疫情防控一线的武汉,其困难程度可想而知。不过,科研攻关团队克服了重重阻力,确保了疫苗研发进度的有序推进。
首先是人员返岗方面的挑战。1月23日,农历腊月29,武汉宣布封城。当时武汉生物制品研究所的一些外地员工,已经回到故乡过年。2月1日,研发工作紧急立项时,只有一半的员工可以到岗。疫情期间,如何重返工作岗位,是摆在许多外地员工面前的难题。
春节前,武汉生物制品研究所的方习静回到了安徽淮南的家中,随着疫情的发展,课题组的一些同事陆续回到实验室,开展应急科研攻关。方习静心急如焚——她负责的工作,关系着质量控制的关键环节。
为了尽快返回工作岗位,方习静第一时间联系公司开具防疫工作证明,多次联系居住社区办理返回武汉申请。2月19日早上6点,她登上了G1741次高铁。不过,受疫情影响,该次高铁不经停武汉,需要到岳阳再想办法回武汉,当列车长得知她的工作情况后,为她在武汉进行了技术特停。当晚11点,方习静拉着行李箱回到实验室,马上投入到了紧张的科研工作中。

正在科研岗位上忙碌的方习静。
像方习静这样的科研人员还有很多。身处外地的武汉生物制品研究所的员工们,克服了重重阻力,经历各种曲折,从四面八方向武汉陆续集结,到2月20日左右,科研骨干基本到齐,为后续研发的快速推进提供了人才支撑。
回到武汉,只是克服困难的第一步,在疫情防控一线的武汉开展研发工作,还面临着工作和生活等方面的其他困难。
比如,在交通方面,日常出行存在困难。由于当时武汉疫情严重,城市交通管控十分严格,不同区域之间的管控政策又不尽相同,且经常调整,这使得科研团队在日常通行方面,需要花费许多沟通和协调的时间成本,保障出行安全顺利。
再比如,生活方面,吃饭就是一大难题。随着疫情的蔓延,武汉的许多饭店和超市纷纷关闭,科研团队的正常就餐成为新的问题。“开始的那段时间,我们成箱成箱地吃泡面。后来单位的后勤帮我们想了很多办法,情况才开始有所缓解。”王泽鋆说。
未来可期:早日完成临床试验尽快制备安全有效的疫苗
4月12日,由国药集团中国生物武汉生物制品研究所申报的一类新药——新型冠状病毒灭活疫苗,获得国家药品监督管理局临床试验许可。消息见诸媒体后,引起了舆论热议,网友们也纷纷留言,表达对央企勇担责任的敬佩之情。
“武汉处在疫情最前沿,武汉生物所也战斗在疫情最前线,一代年轻的科技工作者在老专家的带领下,薪火相传,硕果累累,向他们致敬!”
“央企人坚持科技融入,科技助力,将科学技术作为最有利的武器,给全球战疫打了一针‘强心剂!’”
“全体国药人多少个日夜的不懈努力,奋战在一线!不负使命,造福人类,央企担当!”
据有关专家介绍,灭活疫苗是指通过物理或者化学处理等方法,使病毒失去感染性和复制力,但保留了病毒能引起人体免疫应答的活性而制备成的疫苗。同其它类型的疫苗相比,灭活疫苗研发技术先进、生产工艺成熟、质量标准可控、保护效果良好。
中国生物有关负责人指出,国药集团中国生物具备大规模灭活疫苗生产能力,申报新冠疫苗临床试验批次产量超过5万剂,量产后每批次产量超过300万剂,年产能1亿剂以上。此次成功获得临床试验许可,将进一步为新冠病毒灭活疫苗的“高速”开跑奠定基础。

4月10日,工作人员在国药集团中国生物新冠疫苗生产基地尚未投产的新型冠状病毒灭活疫苗生产车间内调试设备。
目前,该疫苗的临床试验已同步启动。同时,根据国家相关法律法规规定,中国生物已为应急使用做好充分准备。
值得注意的是,该疫苗的一期、二期临床试验是合并进行的。王泽鋆告诉记者,这主要是因为武汉生物制品研究所临床前研究的数据较为充分,同时,当前疫情防控形势依然紧张,因此国家药监局开通了“绿色通道”,一次性批准了两期临床试验。

新型冠状病毒灭活疫苗的相关临床试验已经启动
王泽鋆表示,在当前疫情全球蔓延的情况下,疫苗的三期临床试验,将采取国际多中心的临床试验方式,从而在不同的人种和群体中,评价疫苗的有效性。
国药集团中国生物相关负责人表示,下一步,中国生物将全力以赴、争分夺秒,加速科研攻关,力争早日完成新型冠状病毒灭活疫苗的临床试验研究,尽快制备出安全有效的新冠疫苗,在投入应急使用的基础上,大规模投放市场,满足国内国际需要,为战胜新冠疫情、保障人类公共卫生安全作出新的贡献。(撰稿:国资报告 原诗萌)